科室医生 查看全部
-
中医妇产科

郭晓青
主任医师
科主任
中医妇产科
赵粉琴
副主任医师 副教授
3.5
中医妇产科
李明兰
副主任医师
3.5
中医妇产科
武权生
副主任医师 副教授
3.3
中医妇产科
刘恒瑞
主任医师
3.2
中医妇产科
华红
副主任医师 副教授
3.2
中医妇产科
王玮
副主任医师
3.2
中医妇产科
张小花
副主任医师
3.2
中医妇产科
彭凤娣
副主任医师
3.2
中医妇产科
韩迎娣
主治医师 讲师
3.2
-
中医妇产科

郭月季
主任医师
3.2
中医妇产科
申剑
主治医师
3.2
中医妇产科
梁莉
主治医师
3.2
中医妇产科
张瑞芳
主治医师
3.2
中医妇产科
叶秋香
副主任医师
3.1
中医妇产科
谢知慧
主治医师
3.1
中医妇产科
张苹
3.1
中医妇产科
程芳
医师 助教
3.1
中医妇产科
杨亚玲
3.1
中医妇产科
冯明霞
医师
3.1
科普·直播义诊专区 查看全部
- 精选 宫颈HPV感染治疗指导
1病例一 小王, 女33岁 已婚未孕。于2015-9-11就诊。 2014年1月体检发现HPV16型阳性, TCT 阴性。因为是单纯HPV感染,医生建议阴道用干扰素, 同房用工具套, 观察一年复查。2015年1月份复查HPV16型仍然是阳性, TCT 显示:非典型细胞,不明确意义(ASCUS). 阴道镜下多点活检显示CIN I。医生建议宫颈物理治疗 。 本人考虑尚未怀孕,不愿意做治疗,仍旧观察,间断阴道用干扰素, 锻炼身体提高免疫能力。因为计划怀孕,故今年9月份再次复查: TCT显示仍然为ASCUS, HPV16型仍然阳性, 再次阴道镜下做四个点活检,其中6点和12点显示为CIN 2 ,当地医生建议宫颈LEEP手术。 前来就诊的目的是:咨询是否可以不手术,先怀孕生育后再手术。另外有没有快速去除HPV的办法? 2病例二 李女士 53岁,2013年底因为月经不规则(绝经过渡期),做TCT检查为阴性,HPV16型感染。 尊当地医生医嘱,阴道用干扰素3个月, 观察, 一年后复查。此后月经不规则的情况消失了(已绝经一年半), 就没有按时复查。 2015年8月份在女儿的催促下, 复查TCT为低度病变, HPV16型仍旧阳性, 做阴道镜下多点活检显示: 3点、6点、9点为CIN 2/3,12点为CIN 1。 来就诊的目的是:了解下一步怎么办? 点评 HPV16型属于高危型病毒之一, 与HPV 18型一样,其致癌的能力强,是十几种高危型里面致癌能力最强的类型。因此国际通行的宫颈阴道镜病理协会ASCCP指南建议:对HPV6型和18型感染,尽管TCT阴性, 也建议做阴道镜检查, 必要时进行宫颈多点活检, 以除外宫颈高度病变。 而对其它高危类型的感染,可以观察一年,然后复查TCT和HPV。 HPV感染的清除,主要依靠感染者自身免疫能力,大约经过8-14个月的时间,有80%的人HPV可以自行消失。另外20%的患者,HPV可能持续存在。感染超过一年者,我们称之为“HPV持续感染”。持续感染者,发生宫颈癌前病变的看机会增加。 宫颈癌前病变可以人为地分成3个阶段, 即CIN1, CIN2,CIN3。到了 CIN 3的阶段,如果病变继续发展,就可能成为真正的宫颈癌。宫颈癌前病变的进展,平均每一个阶段大约需要3-5年的时间。但是研究显示,宫颈HPV16型的致癌能力强,自然消退的机会较少,一旦导致癌前病变发生,其进展的速度较快。 从以上2个病例来看, 病人发现了HPV感染之后,都选择了观察,用干扰素的作用是很微小的, 研究显示应用干扰素和不用干扰素比较,只有10%左右的益处。两位患者都经过将近2年的时间,都由单纯的HPV16型感染发展为高度病变 (CIN 2和CIN 3 为高度病变)。当宫颈高度癌前病变发生之后, 自然消退的机会非常小 (年龄小于24岁者除外), 应当采取适当的切除性治疗 (Excision), 切除癌前病变的组织, HPV病毒也可能通过切除病变组织而消除干净, 也即“治病即治毒”。 第一例患者, 因为想要孩子,迟迟不予治疗, 甚至发展到CIN 2, 也不想治疗,是对病情的认识不足,是对自己生命的不负责任。 她在2015年初,发现宫颈CIN1 的时候, 应该予以宫颈表面物理治疗(Ablation),即宫颈激光或电灼术,可以有效地去除病变和病毒,治愈效果达85%左右,并且不影响生育。 她可于月经干净后3-7天, 不同房,去医院做这个手术。这只是一个小的治疗,不需要住院, 不影响生育能力。 现在发展到CIN 2, 她应当采用宫颈切除性治疗, 即宫颈LEEP 或者小的锥切, 切除部分宫颈,可以达到80-90%的治愈效果,并且不会影响妊娠。她可于月经干净后3-7天, 不同房,去医院做这个手术。 宫颈LEEP也是一个小的门诊手术,做完后3个月复查TCT和HPV,如果阴性,她就可以试着怀孕了! 反之如果她还是不去采取积极的治疗方法切除CIN2病变,一两年的时间里,可能会出现CIN3,甚至发展到癌,那时候,就要做大的手术,保留生殖功能就困难了。假如她带着CIN2的病变怀孕,在孕期10个月的时间里,病变可能会进展,带来不可免回的生命危险。 第二个病例,发现了HPV6型感染后,应定期复查TCT和HPV,必要的时候做阴道镜下多点活检。切忌不可忽略不管。幸亏她的女儿关心她,强迫她去复查,及时地发现了高度病变,没有耽搁到癌的出现。她只要住院做个锥切,病变通常就会治愈。 切下来的标本要仔细多点取材,看看有没有忽略掉癌的可能,切缘有没有干净。如果病理显示没有癌,并且切缘干净了,她的病通过锥切就可以治愈了。如果病理显示有癌,或者切缘有高度病变提示残留,她需要进一步手术。 总之, 对于HPV16型感染, 由于病毒较强的致癌能力,由于病毒不易自然消退,我们不能掉以轻心,不能像其它类型的病毒一样处理,而是应当更积极的观察或者治疗。 北京协和医院 孙晓光教授 专家介绍 孙晓光,主任医师,副教授,美国纽约大学做博士后,从事妇产科临床工作30年。对反复流产有丰富的诊治经验,能够对80%以上患者查明原因并获得75%成功率。对不孕症和其他妇科疑难杂症有丰富的临床诊治经验。
赵粉琴 副主任医师 甘肃中医药大学附属医院 妇产科5079人已读 - 精选 孕期能否做MIR检查
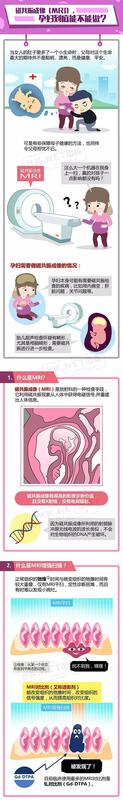
孕检遇到磁共振(MRI),到底能不能做?父母都希望宝宝生出来是健康平安的,于是有些孕期的检查不得不做。可是有一种检查却令准妈妈们犹豫,那就是MRI。它有什么用?会不会对孕妇和孩子造成伤害呢?前三个月原
 赵粉琴 副主任医师 甘肃中医药大学附属医院 妇产科1562人已读
赵粉琴 副主任医师 甘肃中医药大学附属医院 妇产科1562人已读 - 子宫肌瘤治疗后复发诊疗策略
本文刊登于《中国实用妇科与产科杂志》2016年11期1064-1068页 作者:范文生,孟元光 作者单位:解放军总医院妇产科,北京 子宫肌瘤为妇科常见病,是一种激素依赖性肿瘤,孕期生长较快而绝经后萎缩,雌孕激素在子宫肌瘤生长过程中起关键作用。此外,子宫肌瘤的生长和复发机制与芳香化酶、多种细胞因子、表皮生长因子、单核细胞趋化蛋白和细胞外基质等也有关。据报道,子宫肌瘤剔除术后在第1、3、5和8年的肌瘤复发率分别为11.7%、36.1%、52.9%和84.4%。子宫肌瘤术后复发是指术后6个月新发现子宫肌瘤(直径>1 cm)者,经由盆腔超声、妇科检查或其他手术证实。新的子宫肌瘤分期,更明确肌瘤的部位以及与子宫内膜的关系,对治疗方案的选择有更好的指导意义。 1 子宫肌瘤治疗后复发的危险因素 1.1 年龄 子宫肌瘤的复发与年龄呈正相关性,研究认为生育期晚期妇女体内相关激素和生长因子会促进子宫肌瘤生长,在20~30年的雌孕激素持续刺激下子宫肌瘤在生育期晚期易明显增大。 1.2 初次手术肌瘤数目及大小 单发肌瘤复发风险较多发肌瘤低,但是肌瘤直径大于10 cm时,复发可能性增大。初次手术发现肌瘤数目越多,手术完全剔除肌瘤的困难也就越大,且当肌瘤直径35岁、BMI>25、应用过促性腺激素释放激素激动剂(GnRH-a)治疗、多发肌瘤(>2个)、肌瘤直径>10 cm,复发的危险性增加。术后5年的复发率为62.1%,再手术率只有2.4%。因为,大部分复发性子宫肌瘤较小且没有临床症状。 2 初始治疗与复发相关性 2.1 手术治疗 子宫肌瘤剔除术的手术入路选择不恰当易导致肌瘤残留而生长复发。腹腔镜手术视觉效果满意,但触觉差,容易导致深部小肌瘤残留,适于肌瘤数≤3枚者,术中超声监测有助于减少残留;经阴道手术适于经产妇,肌瘤集中于前壁或后壁,肌瘤直径<8 cm,数量<3枚者;经腹手术最经典,而且触觉、视觉效果均最佳,可以最大限度减少残留风险,但创伤大。术前应充分评估患者病情,恰当选择手术入路,在达到治疗目的同时减少复发风险。 2.2 介入治疗 包括子宫动脉栓塞、肌瘤消融技术、超声聚焦刀等微创介入疗法近年应用逐渐增多,被认为是取代肌瘤剔除术及子宫切除术的有效治疗手段,但其长期疗效仍值得继续观察。Spies等统计介入治疗1年后87%患者症状缓解,12%患者治疗失败或无效;5年后73%症状与治疗前相比仍缓解,25%患者治疗无效、病情加重或复发。 2.3 药物治疗 GnRH-a可以缩小肌瘤体积,缓解贫血,为手术做准备。Fedele等研究证实给予GnRH-a后如未及时手术,缩小的子宫肌瘤体积可在短期内复发;另外,术前GnRH-a治疗可能会使一些肌瘤术中难以发现,增加肌瘤复发机会。因此,除大肌瘤伴严重出血患者外,术前应用GnRH-a仍有一定争议。 3 子宫肌瘤的国际妇产科联盟(FIGO)分期 子宫肌瘤新分期:黏膜下肌瘤、非黏膜下肌瘤、混合瘤。通常以数字0~8表示。黏膜下肌瘤:0:有蒂的黏膜下肌瘤;1:内凸>50%的黏膜下肌瘤;2:内凸≤50%的黏膜下肌瘤。非黏膜下肌瘤:3:表面覆盖子宫内膜的肌壁间肌瘤;4:完全性肌壁间肌瘤;5:外凸≤50%的浆膜下肌瘤;6:外凸>50%的浆膜下肌瘤;7:有蒂的浆膜下肌瘤;8:其他(特殊类型的子宫肌瘤,比如宫颈肌瘤,寄生瘤)。混合瘤(同时累及子宫内膜和浆膜层的子宫肌瘤):用两个以连字符-连接起来的数字来表示,通常第一数字表示肌瘤与子宫内膜的关系,后一个数字表示肌瘤与浆膜的关系。例如:2-5:肌瘤内凸向宫腔外凸向浆膜但均不超过其直径的50%。 新的FIGO分期,可以更加明确子宫肌瘤的部位以及与子宫内膜的关系,数字越小,肌瘤越靠近子宫内膜;越大,越靠近子宫浆膜。混合瘤的命名,较过去的多发性子宫肌瘤更明确肌瘤部位和可能产生的症状及影响。缺点是仍然不能体现肌瘤大小和子宫大小。 4 复发性子宫肌瘤的病理特征 当复发性子宫肌瘤出现类似于平滑肌肉瘤、子宫内膜间质肉瘤的组织形态和生长方式却又不具有典型恶性的组织学特征时,往往会引起诊断困难。这些肿瘤细胞可带有异型性、核分裂象等非良性特征,但又不具有中重度核异型性+大量核分裂象+凝固性坏死的典型恶性特征,此时应结合临床表现,动态观察肿瘤的生物学行为和病情发展作出综合判断。目前,将交界性子宫肌瘤分为下列几种:富于细胞性平滑肌瘤、弥漫性平滑肌瘤病、分割状平滑肌瘤、多形性平滑肌瘤、核分裂活跃的平滑肌瘤、上皮样平滑肌瘤、不能确定恶性潜能的平滑肌肿瘤。这些病理类型术前的临床表现和影像学特点与子宫平滑肌瘤很难区分,多在术后病理检查时诊断。对于此类复发病例,应核实初次手术病理,将富于细胞性、异型性、核分裂象活跃和凝固性坏死列为交界性子宫肌瘤的四大诊断指征,再结合雌激素受体(ER)、孕激素受体(PR)、增殖细胞核抗原(proliferating cell nuclear antigen,PCNA)和p53的检测做出综合判断,治疗上以根治性手术为主,防止肉瘤变的发生。 5 复发性子宫肌瘤的治疗策略 复发性子宫肌瘤的治疗原则应以解除症状和根治疾病为主,根据不同患者具体情况制定个体化治疗方案。年龄、孕产次、生育需求、临床症状严重程度,肌瘤分期,相关医疗条件,恶变风险,近绝经期等是主要影响治疗的因素。治疗方法包括:随诊观察、药物治疗和手术治疗。手术治疗分为保留子宫的保守手术与子宫切除术。子宫肌瘤FIGO新分期对治疗选择有重要意义。 5.1 黏膜下子宫肌瘤 初次手术选择腹腔镜入路者,容易导致深在小肌瘤残留,术后严密随诊。当出现月经过多,应考虑是否有残留肌瘤继续长大凸向宫腔,0型与1型子宫肌瘤,可考虑直接行宫腔镜手术;2型子宫肌瘤,如瘤体较大,超过3~4 cm,建议应用GnRH-a缩小瘤体后再行宫腔镜手术。黏膜下子宫肌瘤常会引起继发不孕或导致流产,所以宫腔镜下肌瘤切除术常用于肌瘤致宫腔形态失常而引起的辅助生殖失败患者的治疗。 5.2 非黏膜下子宫肌瘤 定期随诊是大多数复发性子宫肌瘤患者的主要处理方法。复发患者若为非黏膜下子宫肌瘤5~7型,大多无明显临床症状,对肌瘤较小、不影响日常生活者可定期随诊。随诊间隔一般为3~6个月,期间注意有无前述症状出现和加重,注意动态观察子宫体积变化,通常行妇科检查并辅以超声检查。很多近绝经期的复发患者往往具有手术或治疗指征,但由于临床症状不明显、有保留子宫的强烈意愿、手术耐受性差或心理因素等选择随访观察。对于近绝经期复发性子宫肌瘤患者GnRH-a治疗也可以在一定程度上减少手术的需求。 对于3、4型子宫肌瘤,当出现异常子宫出血加重或慢性子宫失血导致继发性贫血者,建议行诊断性刮宫排除子宫内膜病变。肌瘤较大或者多发肌瘤子宫整体大于孕10周,应该考虑子宫切除。用于治疗复发性子宫肌瘤的药物有:GnRH拮抗剂、芳香化酶抑制剂、选择性雌激素受体修饰剂、抗孕激素制剂(米非司酮)、选择性孕激素受体修饰剂和左炔孕酮缓释装置(宫内节育器)等。但这些药物的作用机制及临床应用效果还需进一步验证。 肌瘤较大的患者,可以术前采用GnRH-a治疗。它能在垂体水平下调GnRH受体,抑制卵巢激素产生,达到降低雌激素的目的,既可用于术后预防复发,也可用于术前辅助治疗。GnRH-a治疗所致人工闭经可改善贫血,减少术中出血,利于子宫肌瘤剔除手术和宫腔镜黏膜下肌瘤切除手术进行。术前使用GnRH-a治疗3个月后子宫肌瘤体积可减小35%~65%。因此,应用GnRH-a最主要的指征是术前预处理。值得注意的是,GnRH-a治疗后肌瘤会萎缩变软,与正常肌层的层次变得不清楚,有时会造成手术剥离困难,故术前应用不宜超过3个月。 5.3 其他部位的子宫肌瘤 8型子宫肌瘤,宫颈肌瘤或阔韧带肌瘤,大于3 cm,就建议手术治疗。因为这些部位的肌瘤生长过大会压迫输尿管,引起输尿管扩张、肾积水,给手术带来困难。手术入路可以腹腔镜或经阴道手术,手术困难时可以考虑开腹手术。 5.4 混合瘤 当复发性子宫肌瘤为混合瘤,处理原则与肌瘤大小及分期有关。 如果肌瘤不大,其中为0、1、2型的部分,一般会引起月经过多,淋漓不尽,容易合并感染,可以只做宫腔镜解决黏膜下肌瘤;5、6、7型的部分,一般无症状,可以随诊观察;而3、4型的部分,要根据患者症状决定治疗,当合并月经过多时,要注意有无子宫内膜增厚的问题,诊断性刮宫排除内膜病变后,可以观察。比如2-4型混合瘤,有时在宫腔镜解决2型部分的肌瘤后,4型的部分会演变为3型或者2型,可以在宫腔镜手术3个月后复查,酌情再次行宫腔镜手术。 如果肌瘤较大,单个肌瘤超过5 cm,或者多发肌瘤整体超过孕10周,如1-6型,应该考虑子宫切除术。复发性2-4型子宫肌瘤较为常见,较大的肌瘤可能合并某种肌瘤变性,腹腔镜下子宫均匀增大、变软,没有超声监视,很难找到肌瘤位置,故建议做全子宫切除术。 6 复发性子宫肌瘤的手术抉择 6.1 肌瘤剔除术与子宫切除术的抉择 对于复发性子宫肌瘤是否保留子宫,要根据患者的年龄、是否有生育要求,上次手术病理结果、子宫肌瘤分期、子宫大小、肌瘤增长速度、是否合并贫血,超声、磁共振(MRI)等检查结果中肌瘤的特征,以及征求患者的意愿等进行综合判断。 对于年轻、希望保留子宫,尤其是未生育的非黏膜下子宫肌瘤患者,尽量行子宫肌瘤剔除术,通常二次手术选择经腹手术成功率较高,因为前次手术造成的腹腔内粘连导致腹腔镜或经阴手术中转开腹率增加。而黏膜下子宫肌瘤,多采用宫腔镜手术。 对于复发性子宫肌瘤患者,在选择肌瘤剔除术前应进行全面的术前评估:首先排除宫颈病变;有月经不调病史或内膜病变者需行宫腔镜手术明确内膜病变性质,尤其对于年龄超过35岁者;对于贫血患者应药物治疗或输血以改善症状,术前积极备血。 对于混合瘤,特别是越接近子宫内膜的多发肌瘤,年龄较大(超过45岁)、无生育要求、复发较快、临床症状明显以及上次病理结果为富于细胞性平滑肌瘤,手术宜选择全子宫切除术。因为有过腹部手术史,可能存在盆腔或肠管粘连,手术入路以开腹或腹腔镜辅助经阴道子宫切除为宜。 6.2 子宫切除术入路的选择 子宫切除术是根治子宫肌瘤的方法,也是复发性子宫肌瘤手术治疗最常用的方法。 根据不同的手术入路,分为经腹子宫切除术(TAH)、阴式子宫切除术(TVH)、腹腔镜子宫切除术(LH)3种,临床选择手术入路时应从手术的有效性、安全性和术者擅长等方面综合考虑。 6.2.1 TAH 直视下术野暴露好,手术操作精巧、细致、可同时处理并存的盆腔及附件病变;TAH最大缺点是创伤大,康复慢。 6.2.2 TVH 因为子宫动脉位置较低,阴式子宫切除较早切断子宫血管,手术出血少;对于子宫直肠窝的粘连,阴式手术更容易贴近子宫找到子宫直肠间隙,避免肠管损伤。因此,阴式子宫切除具有创伤小,康复快且手术费用低等优点;但经阴道手术术野暴露有限,不能处理所有盆腔病变。 6.2.3 LH 腹腔镜子宫切除术因其微创特点而被广泛接受,具有切口小、恢复快、术后并发症发生率低的优点;在施行腹腔镜子宫切除术时,还可实施其他疾病如子宫内膜异位病灶清除、卵巢肿瘤切除、阴道断端悬吊、盆底缺陷修补等手术。对合并盆腔粘连、子宫内膜异位症、卵巢肿瘤等病变而需切除子宫者,腹腔镜手术应作为首选。 解放军总医院通过对多年经阴道子宫切除手术的对比研究,认为超大体积或粘连严重的子宫切除,腹腔镜联合阴式手术,既可以发挥腹腔镜术野清晰全面,又可以借助阴式手术处理子宫血管韧带快捷、可靠的优点,增加了子宫的活动性,减少了腹腔镜下的盲区,提高了手术效率,减少中转开腹的发生率。 6.3 是否保留宫颈问题 根据是否保留宫颈,分为全子宫切除术和次全子宫切除术。全子宫切除术切除了有可能发生宫颈病变甚至癌变的子宫颈,但术中膀胱及输尿管损伤的发生率升高,也会增加阴道穹窿脱垂发生率;次全子宫切除术在子宫峡部或稍上方切除子宫体,保留宫颈血供及其生理功能,与全子宫切除术比较可以减少术中泌尿系副损伤和盆底功能损伤。子宫切除手术时是否需要保留宫颈没有明确指征,然而由于存在发生宫颈病变甚至宫颈癌的风险,残留宫颈对于患者和医生都是一种心理负担。由于子宫肌瘤患者常合并子宫内膜异位症、子宫腺肌病、宫颈病变、子宫内膜病变或卵巢病变等,因此复发性子宫肌瘤患者要通过查体和辅助检查充分评估病情、鉴别诊断,抓住主要问题,综合处理。对于有其他合并症的复发患者可以适当放宽全子宫切除术的手术指征,一次手术解决多个问题。 随着现代医学的发展和精准医疗理念的推广,为复发性子宫肌瘤的诊治提出了更高要求。在规范化、人性化和微创化的初治原则下,保留子宫的微创手术如腹腔镜子宫肌瘤剔除术和宫腔镜子宫肌瘤切除术成为重要选择,药物治疗和介入治疗也占有一席之地。因此,子宫肌瘤初治后的复发问题日益受到关注,对于复发性子宫肌瘤患者,诊断后应密切随访,处理原则和初治患者要有所区别,应以解除症状和根治疾病为目的,为每一位复发患者量体裁衣,做出精准、个体化的临床决策。内容转载自公众号 中国实用妇科与产科杂志
赵粉琴 副主任医师 甘肃中医药大学附属医院 妇产科2660人已读
问诊记录 查看全部
- 月经提前 二胎宝宝目前1岁10月,近两月,月经提前一周,月经量正常 药物治疗总交流次数14已给处置建议
- 月经不调 近半年月经不调,上个月例假是1.26日来的,2.11的时候就... 请问该如何继续服药,服哪个方子呢?总交流次数13已给处置建议
- 患者:女 22岁 痛经十余年 最后交流时间 2020.10.08痛经十余年 喝了药喉咙痛总交流次数8已给处置建议
- 妇科内分泌 因为月经量变少,就医后服用克龄 咨询是什么原因导致停药第十天了还没有来姨妈总交流次数11
- 保胎中,孕早期出血,b超可以看见胎芽胎心 目前保胎中,4月30号出血,5月1号 可以去门诊总交流次数10



